صواب أم خطأ
أمثلة على تفاعلات ماصة وطاردة للحرارة, إشارة التفاعل الطارد للحرارة, المعادلة الكيميائية التالية تمثل تفاعل طارد للطاقة حرارة 4Fe 3o3 → 2FeO3, جدول مقارنة بين التفاعلات الطاردة والماصَّة للحرارة, عندما يطلق حرارة في التفاعلات الطاردة للحرارة تكون طاقة الروابط في النواتج, في التفاعلات الطاردة للحرارة تكون طاقة, معادلة تفاعل طارد للحرارة
فريق خبرمكس
0 تعليقات
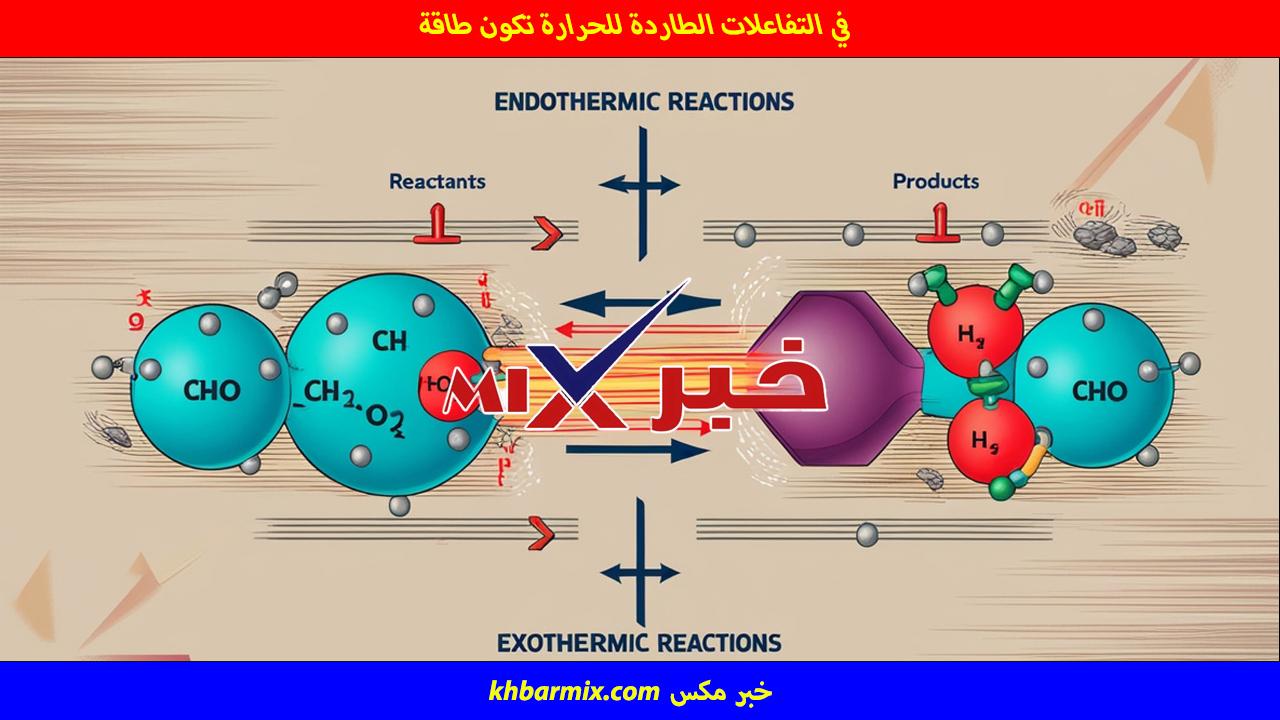
في التفاعلات الطاردة للحرارة تكون طاقة صواب أم خطأ
في التفاعلات الطاردة للحرارة تكون طاقة | تُعد التفاعلات الكيميائية من أهم الموضوعات التي يدرسها الطلاب في مادتي العلوم والكيمياء، خصوصًا عند الحديث عن الطاقة والتغيرات المصاحبة للتفاعل. ومن أكثر الأسئلة الشائعة التي تتكرر في الاختبارات النهائية، وخاصة في قسم صواب أم خطأ، وللإجابة الصحيحة عن هذا السؤال، يجب أولًا أن نفهم مفهوم التفاعلات الطاردة للحرارة، وما الذي يحدث للطاقة خلالها، وكيف يمكن تمييزها بسهولة أثناء المراجعة.
ما المقصود بالتفاعلات الطاردة للحرارة؟
التفاعلات الطاردة للحرارة هي نوع من التفاعلات الكيميائية التي يتم خلالها انطلاق طاقة حرارية إلى الوسط المحيط أثناء حدوث التفاعل. بمعنى آخر، التفاعل لا يستهلك حرارة من البيئة، بل يُنتج حرارة نشعر بها أو نقيسها. ومن أمثلة ذلك:
- احتراق الوقود
- احتراق الشمعة
- تفاعل الأحماض مع القواعد
- تفاعل الصوديوم مع الماء (مع الانتباه لخطورة التجربة)
في التفاعلات الطاردة للحرارة تكون طاقة ماذا؟
الإجابة العلمية الدقيقة هي: في التفاعلات الطاردة للحرارة تكون طاقة المتفاعلات أكبر من طاقة النواتج. وهذا هو الأساس الذي تُبنى عليه معظم أسئلة صواب وخطأ في هذا الدرس. لماذا؟ لأن:
- المتفاعلات تحتوي على طاقة مخزنة أعلى
- أثناء التفاعل، يتم تحرير جزء من هذه الطاقة
- تنتقل الطاقة الزائدة إلى الوسط المحيط على شكل حرارة
- تصبح طاقة النواتج أقل من طاقة المتفاعلات
الصيغة الصحيحة لسؤال صواب أو خطأ
- عند ورود السؤال في الامتحان بصيغة: «في التفاعلات الطاردة للحرارة تكون طاقة المتفاعلات أقل من طاقة النواتج» الإجابة: خطأ والتصويب هو: في التفاعلات الطاردة للحرارة تكون طاقة المتفاعلات أكبر من طاقة النواتج.
- أما إذا جاء السؤال كالتالي: «في التفاعلات الطاردة للحرارة تكون طاقة المتفاعلات أكبر من طاقة النواتج» الإجابة: صواب العلاقة بين التفاعلات الطاردة للحرارة والطاقة
لفهم هذا الدرس بشكل أعمق، يجب التركيز على مفهوم حفظ الطاقة، حيث إن الطاقة لا تفنى ولا تُستحدث من العدم، وإنما تتحول من شكل إلى آخر.
في التفاعلات الطاردة للحرارة:
- تتحول الطاقة الكيميائية إلى طاقة حرارية
- تظهر الحرارة كنتيجة مباشرة للتفاعل
- ترتفع درجة حرارة الوسط المحيط
وهذا ما يميزها عن التفاعلات الماصة للحرارة التي يحدث فيها العكس تمامًا.
مقارنة بين التفاعلات الطاردة والماصة للحرارة
| وجه المقارنة | التفاعلات الطاردة للحرارة | التفاعلات الماصة للحرارة |
| اتجاه الطاقة | تنطلق إلى الوسط المحيط | تمتص من الوسط المحيط |
| طاقة المتفاعلات | أكبر | أقل |
| طاقة النواتج | أقل | أكبر |
| درجة الحرارة | ترتفع | تنخفض |
| علامة ΔH | سالبة | موجبة |
لماذا يركّز المنهج على هذا السؤال؟
هذا السؤال يُعد من:
- الأسئلة المفاهيمية الأساسية
- الأسئلة المتكررة في الامتحانات النهائية
- الأسئلة التي تقيس الفهم وليس الحفظ فقط
لذلك، فإن فهم العلاقة بين الطاقة والمتفاعلات والنواتج يُجنب الطالب الوقوع في أخطاء شائعة أثناء الاختبار.
أخطاء شائعة يجب الانتباه لها
من أكثر الأخطاء التي يقع فيها الطلاب:
- الخلط بين الطاردة والماصة للحرارة
- الاعتقاد أن انطلاق الحرارة يعني زيادة طاقة النواتج
- حفظ الإجابة دون فهم السبب العلمي
والحل هو ربط الفكرة دائمًا بجملة ثابتة: إذا انطلقت حرارة → طاقة المتفاعلات أكبر